乳腺癌作为中国女性第一高发恶性肿瘤,发病率呈逐年上升趋势。随着早期筛查技术和综合治疗技术的发展,乳腺癌的疗效得到显著的改善。根据美国国立癌症研究所(NCI)的数据,乳腺癌的五年存活率已达89.9%。尽管这一数字十分可观,但其中一种亚型——“三阴性乳腺癌(TNBC)”却仍旧存在预后差、复发率高、存活率低的问题。这类病例占全部乳腺癌患者的12%~20%。
乳腺癌细胞一般以雌激素受体(ER)、孕激素受体(PR)、人表皮生长因子受体-2(HER2)作为分类依据。对上述某些受体为阳性的患者,改变体内的激素水平,或者施用相应的受体抑制剂,可以抑制乳腺癌细胞和肿瘤的生长,是极为有效的辅助治疗手段。而对三种受体均缺乏的三阴性乳腺癌,意味着针对这几种受体的内分泌治疗和靶向治疗均无效。手术辅助放、化疗仍旧是治疗这种癌症的主要手段。
人们在很多癌细胞(包括三阴性乳腺癌)中都发现了过量表达的组蛋白赖氨酸甲基转移酶EZH2。今日,纽约西奈山伊坎医学院(Icahn School of Medicine at Mount Sinai)的金坚教授课题组与Ramon Parsons教授课题组合作,从这一甲基转移酶入手,首创性开发出EZH2的高效、高选择性且安全的降解剂MS1943,试图以此攻克三阴性乳腺癌的治疗难题。
EZH2是多梳抑制复合体2(PRC2)的重要催化单元,通过催化组蛋白H3第27位赖氨酸(H3K27)的甲基化来调控基因的表达、识别和发展。在以往的研究中,研究人员往往将着眼点放在如何调控EZH2的催化性能。因而之前发展的EZH2抑制剂主要用于抑制H3K27的过量甲基化,对依赖这一过程的弥漫大B细胞淋巴瘤(DLBCL)、恶性横纹肌样瘤(MRT)等癌细胞有很好的抑制作用。研究表明,EZH2除了能催化H3K27的甲基化,还有其他生理作用。在乳腺癌细胞中,EZH2蛋白含量越高,往往预后越差。而乳腺癌细胞却不依赖于下游H3K27的过量甲基化,因而EZH2抑制剂对这种癌细胞无能为力。
作者认为,EZH2蛋白的降解或许是治疗乳腺癌的一种有效手段。遵循这一思路,MS1943成功地选择性降解了EZH2,体外和小鼠体内的活性测试表明,其能有效地杀灭三阴性乳腺癌细胞,抑制肿瘤生长。相关结果发表在Nature旗下子刊Nature Chemical Biology上。
金坚教授课题组长期致力于组蛋白甲基转移酶抑制剂和降解剂的开发。在此项研究中,他们将之前发展的EZH2蛋白抑制剂C24略加改造,修饰一个亲脂性的金刚烷标签,就能利用这个金刚烷标签将EZH2蛋白的空间折叠构象改变,使其被细胞内的蛋白降解酶识别并降解。

研究者首先使用对EZH2敏感的MDA-MB-468三阴性乳腺癌细胞,表征了MS1943在体外对EZH2蛋白的降解活性。在MS1943的作用下,EZH2的含量明显下降,同时,作为EZH2催化功能产物的H3K27me3蛋白含量随之下降。MS1943具有很高的选择性,细胞内的其他蛋白如EZH1以及和EZH2同属多梳抑制复合体2(PRC2)的SUZ12和EED都没有被降解。作为对照,C24高效抑制了EZH2的催化活性,因而H3K27me3蛋白表现出了比MS1943更低的水平;而EZH2蛋白本身和其他蛋白含量都没有明显的降低。
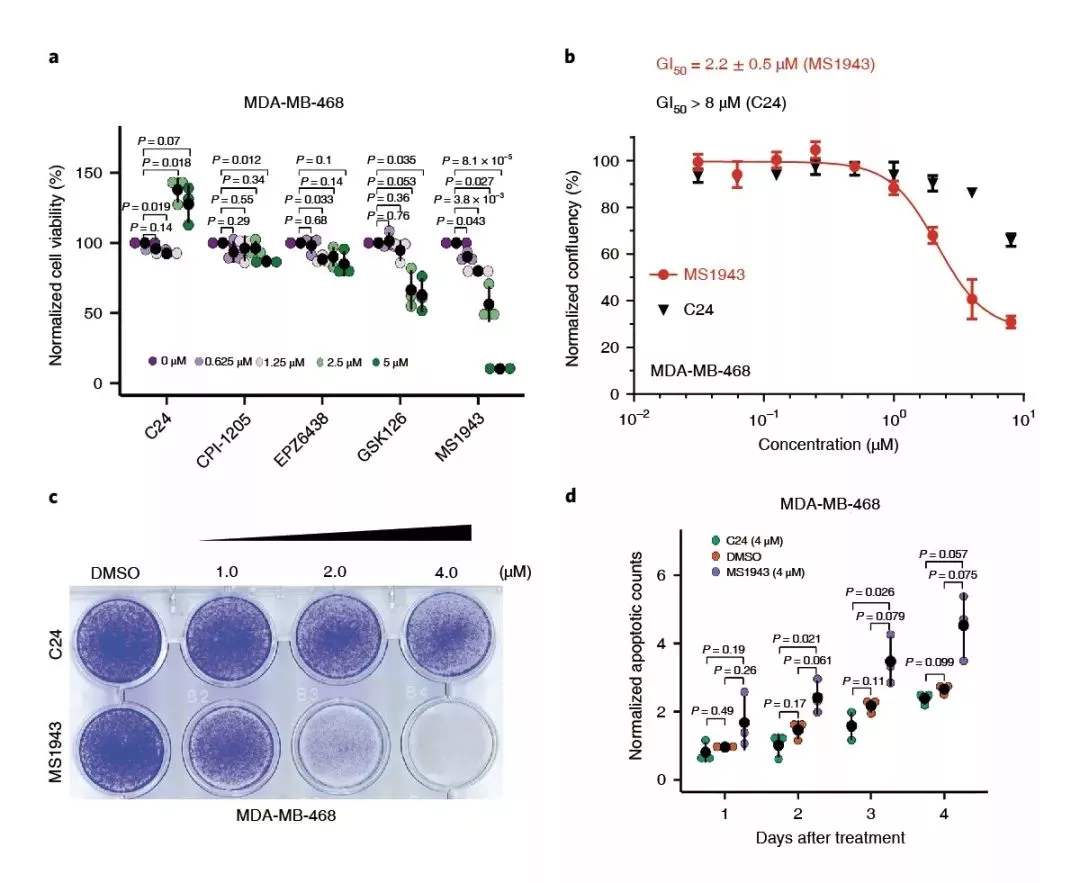
之后,他们考察了MS1943和C24对癌细胞增殖的影响。如下图所示,MS1943在2.2 μM浓度下可以杀灭50%的癌细胞(GI50);而C24虽然能更有效地抑制EZH2的催化活性,其对癌细胞增殖的抑制作用并不明显,GI50超过了8 μM。这与前人的研究结论相吻合,即乳腺癌细胞依赖EZH2蛋白催化作用之外的其他生理功能。活细胞的结晶紫染色试验和死亡细胞的DRAQ7染色试验得到了更直观的结论:在2~4 μM的浓度下,MS1943显著抑制了MDA-MB-468细胞的增殖。
为了证明MS1943是通过降解EZH2导致的细胞毒性,而不是影响了细胞的其他生理功能,研究者使用CRISPR/cas9技术敲除了两种对MS1943敏感的三阴性乳腺癌细胞(BT549 和MDA-MB-468)的EZH2基因。作为对照,他们也敲除了MDA-MB-231这种对MS1943不敏感的癌细胞EZH2基因。如果假设成立,即MS1943是通过降解EZH2来杀灭细胞,那么对MS1943不敏感的细胞对EZH2含量的降低也不敏感。结果与预期十分吻合:BT549和MDA-MB-468这两种对MS1943敏感的细胞增殖受到了很大影响,而MDA-MB-231的细胞增殖不受影响。研究者还通过不同程度抑制MDA-MB-468细胞EZH2基因的表达水平来观察EZH2蛋白水平对细胞增殖的影响:EZH2基因表达越低,细胞增殖的抑制也越严重。
以上研究结果表明,MS1943对某些EZH2敏感的肿瘤具有潜在的治疗效果。
随后,他们表征了MS1943在体内的生理活性。通过给移植了MDA-MB-468肿瘤的小鼠每日腹腔注射一次150 mg/kg剂量的MS1943,肿瘤生长得到完全抑制。在这个剂量下,小鼠并没有表现出体重降低等药理毒性。解析小鼠肿瘤和血浆中的MS1943的含量,其浓度都超过了有效抑制肿瘤细胞的增殖浓度(GI50)。这些事实说明在体内有效剂量的MS1943作用下,小鼠是安全的。
在文章的最后,研究者证明,MS1943通过降解EZH2导致内质网功能持续紊乱,未折叠蛋白质应答过度激活,从而启动癌细胞凋亡程序。这是MS1943有效杀灭三阴性乳腺癌细胞的机制。
EZH2蛋白存在于多种癌细胞中,曾得到了生物医药学界的广泛关注,一系列针对肉瘤、淋巴瘤、恶性横纹肌样瘤的治疗方法都将EZH2作为靶点。然而尽管多个研究表明EZH2在三阴性乳腺癌细胞中也存在过度表达,且其含量与肿瘤体积、癌症分期、癌症预后密切相关,但从未有人将其作为三阴性乳腺癌的靶点进行研究。这可能与各种EZH2抑制剂对三阴性乳腺癌细胞均无效有关。
金坚教授课题组的研究表明,将EZH2作为三阴性乳腺癌的治疗靶点是完全可行的,但是通过抑制其催化活性不能达到抑制癌细胞增殖的目的;将其降解则可以有效抑制肿瘤生长。这为攻克一系列包括三阴性乳腺癌在内的EZH2高表达癌症的治疗难题提供了一个新的思路。




